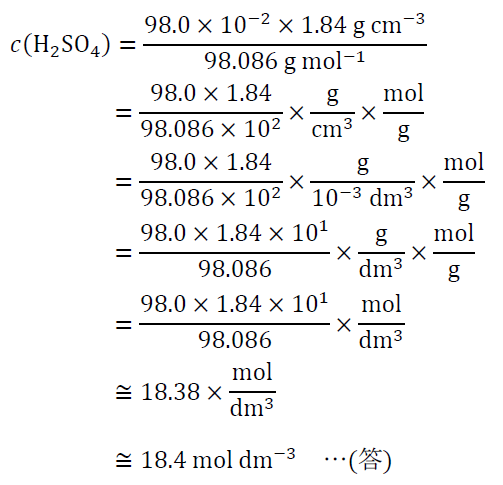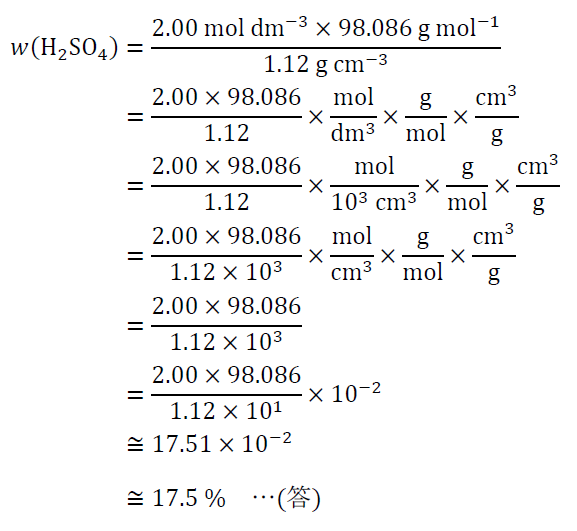0002. 化学(物理化学):物質量濃度と質量分率の換算。
戻る
2024年3月3日掲載
【解説】
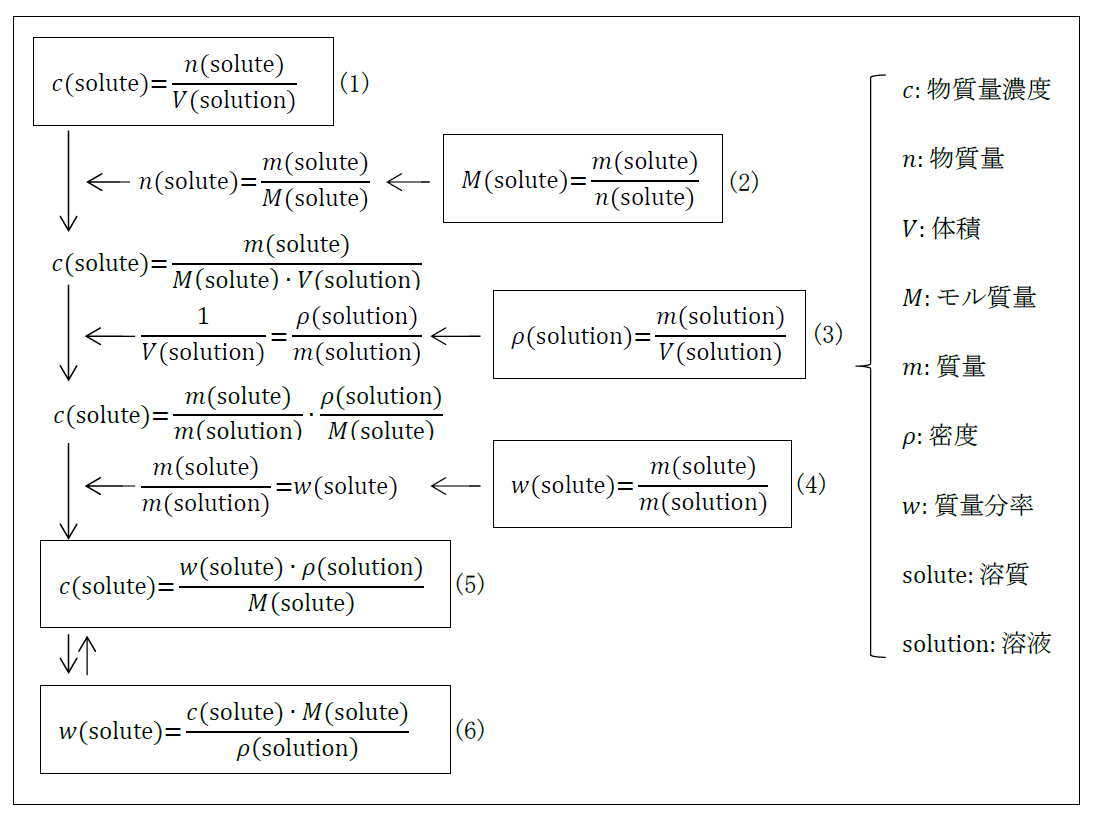
(1)は物質量濃度の定義、(2)はモル質量の定義、(3)は密度の定義、(4)は質量分率の定義である。(1)より、(2)を変形した式を用いて溶質の物質量を消去し、(3)を変形した式を用いて溶液の体積を消去し、(4)を変形した式を用いて溶質および溶液の質量を消去すると、(5)および(6)が得られる。
【(5)の応用例】
質量分率が98.0 %の濃硫酸(密度1.84 g cm-3)の物質量濃度を求める。
溶質(溶媒を含まない純粋な硫酸)のモル質量の値が与えられていないので、まずそれを求める。原子量表(2022)の4桁の原子量の一覧より、H: 1.008、S: 32.07、O: 16.00。よって、硫酸(H2SO4)のモル質量は、
(1.008×2+32.07+16.00×4) g mol-1≒98.086 g mol-1。
よって、(5)より、
なお、これらの公式を用いなくても求められる方法が、高校課程でよく紹介されるので、合わせて紹介しておく。
「溶液の体積を1 dm3と仮定する」のである。
まず、最終的に求める物質量濃度は、
「(物質量濃度)=(溶質の物質量)÷(溶液の体積)」…(7)
であるから、これらを順番に求めていく。今、(溶液の体積)を1 dm3としたので、(7)は、
「(物質量濃度)=(溶質の物質量)÷1 dm3」…(7)'
となる。
(7)'で、割り算の分子の(溶質の物質量)は、モル質量の定義式を変形して、
「(溶質の物質量)=(溶質の質量)÷(溶質のモル質量)」…(8)
で求められる。値を代入すると、
「(溶質の物質量)=(溶質の質量)÷98.086 g mol-1」…(8)'
となる。
さらに(8)'の(溶質の質量)は、今、(溶質の質量分率)が98.0 %と与えられているから、
「(溶質の質量)=(溶質の質量分率)×(溶液の質量)」…(9)
として求められる。値を代入すると、
「(溶質の質量)=98.0×10-2×(溶液の質量)」…(9)'
となる。
ここで、(9)'の(溶液の質量)は、今、(溶液の密度)が1.84 g cm3と与えられているから、
「(溶液の質量)=(溶液の密度)×(溶液の体積)」…(10)
で計算できる。値を代入すると、
「(溶液の質量)=1.84 g cm-3×1 dm3」…(10)'
となる。(10)'を(9)'に代入すると、(溶質の質量)は、
「(溶質の質量)=98.0×10-2×1.84 g cm-3×1 dm3」…(11)
となる。(11)を(8)'に代入すると、(溶質の物質量)は、
「(溶質の物質量)=98.0×10-2×1.84 g cm-3×1 dm3÷98.086 g mol-1」…(12)
となる。これが、(7)'の割り算の分子に相当するから、(12)を(7)'に代入すると、最終的に求める物質量濃度は、
「(物質量濃度)=98.0×10-2×1.84 g cm-3×1 dm3÷98.086 g mol-1÷1 dm3」…(7)''
となり、(7)''中の「1 dm3÷1 dm3」は約分されるから、(7)''は、
「(物質量濃度)=98.0×10-2×1.84 g cm-3÷98.086 g mol-1」…(7)'''
として計算できる。
ここで気をつけねばならないのは、体積の単位として「cm3」((7)'''では、その逆数の「cm-3」)が用いられていることである。通常、物質量濃度の単位には、「mol dm-3」が用いられるので、
「1 dm3=103 cm3」
すなわち、
「cm-3=103 dm-3」
の関係を用いて、(7)'''は、
「(物質量濃度)=98.0×10-2×1.84 g×103 dm-3÷98.086 g mol-1」…(7)''''
すなわち、
「(物質量濃度)=98.0×1.84 g dm-3×101÷98.086 g mol-1」…(7)'''''
となる。
(7)'''''を見れば、やっている計算は、上で公式を用いて求めた方法と同じことがわかる。
(※)なお、日本の初等教育・中等教育において、「'」記号のことを「ダッシュ」と呼ぶことが多いが、これは日本の「方言」で、正確には、ダッシュ(dash)とは長い水平の横棒「-」のことである。「'」は「プライム」(prime)というのが正しい。2つ重ねた「''」は、「ツーダッシュ」ではなく「ダブルプライム」と呼ぶ。以下、「トリプルプライム」(triple prime、3重のプライム)、「クアドループルプライム」(quadruple prime、4重のプライム)、「クインテュープルプライム」(quintuple prime、5重のプライム)、…である。
【(6)の応用例】
物質量濃度が2.00 mol dm-3の希硫酸(密度1.12 g cm-3)の質量分率を求める。
溶質のモル質量は、上の(5)の応用例と同様に、約98.086 g mol-1であるから、(6)より、
戻る
Copyright(C) 2017 KONISHI, Shoichiro. All rights reserved.